코로나19가 장기화된 상황 속에서도 첨단바이오의약품(재생의료) 임상이 전 세계적으로 활발히 진행되고 있다. 이처럼 활발한 임상에 힘입어 올해 미국과 유럽에서 최소 8개의 첨단바이오의약품의 허가가 기대되고 있다.
한국바이오협회는 최근 '재생의료연합(ARM)'의 2020년 연간보고서를 통해 글로벌 첨단바이오의약품의 해외 투자와 임상 현황을 분석했다.
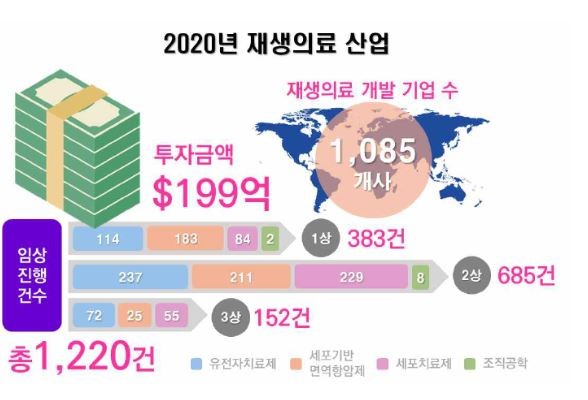
이에 따르면, 2020년 기준 재생의료 개발 기업 수는 1085개사에 달하고 임상에만 1220건이 진행되고 있다. 또 지난 해 코로나19에도 불구하고 재생의료에 199억달러의 자금이 조달되었으며, 관련 기업들의 주가도 강세를 보였다.
재생의료연합(Alliance for Regenerative Medicine, ARM)에 따르면 현재 전 세계적으로 1220건의 재생의료(첨단바이오의약품) 임상이 이뤄지고 있으며, 이중에서 152건이 3상을 진행 중에 있다. 2021년에는 미국, 유럽 등에서 최소 8개의 재생의약품 허가가 기대된다.
보고서는 코로나19에도 불구하고 2020년 재생의료(첨단바이오의약품) 산업은 큰 폭으로 성장했으며 iPSC, 유전자 편집, 동종이계 세포 면역치료 등의 분야에서 성과가 있었다고 분석했다.
미국, 유럽 등 선진국 규제기관에서는 첨단바이오의약품의 신속한 인허가 절차를 지원하는 패스트 트랙제도를 활성화해 기업의 연구개발을 지원하고 있다. 첨단바이오의약품의 개발과 생산을 지원하기 위한 위탁개발생산기업(CDMO)들도 투자를 크게 확대하고 있다.
재생의료란 세포, 조직, 장기 등의 기능을 복원시키는 의학 분야로 난치성 질환의 치료 대안으로 부각되고 있다.재생의료 산업의 범위는 줄기세포치료제, 바이오소재, 조직공학, 면역세포치료제, 유전자치료제 분야를 포함한다.
미국, 유럽 등 선진국에서는 정부 및 민간 투자가 재생의학 시장의 성장 요인으로 작용한다. 코로나19의 영향에도 불구하고 2020년 세계 재생의료산업에 전년대비 50% 증가한 199억달러의 자금이 조달됐다.
2020년 한 해 동안 미 증권 중에서도 재생의료관련주는 강세를 보여 나스닥 지수 대비 큰 폭의 상승을 기록했다. 나스닥바이오지수(NBI)는 연간 23% 증가한 반면 유전자치료제관련주는 70%, 세포기반 면역항암제(IO) 관련주는 82%, 전체 재생의료관련주는 44% 성장했다.
한편 민간 벤처투자금액은 2019년 41억달러였으며 2020년에는 56억달러였다. 시리즈 A 펀딩은 20억달러, 시리즈 B 펀딩은 8억6400만달러, 시리즈 C 펀딩은 6억4200만 달러, 시리즈 D 펀딩은 6억8400만달러가 투자됐다.
벤처기업뿐만 아니라 대형 제약사들도 소형 바이오 회사들과의 파트너십 모색에 나서고 있다. 대표적으로 바이오젠과 상가모의 3억5000만달러 계약, 얀센과 페이트테라퓨틱스 간의 1억달러 계약 등의 성과가 있었다.
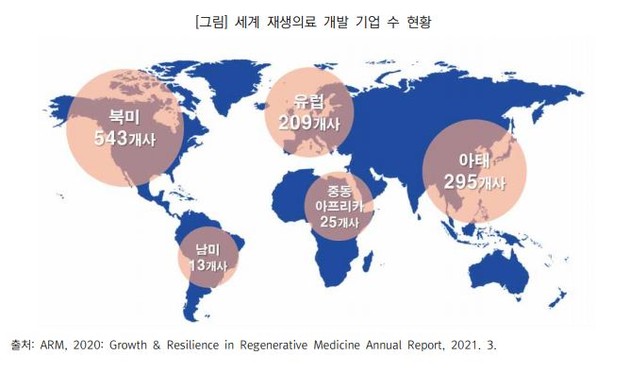
적극적인 투자의 결과로 전 세계 유전체, 세포·조직 기반 치료제를 개발 중인 업체는 2021년 3월 기준 총 1085개로 파악된다.
바이러스 벡터 이용한 백신생산 증가세
코로나19에도 불구하고 2020년 재생의료 산업은 큰 폭으로 성장해 iPSC, 유전자 편집, 동종이계 세포 면역치료 등의 분야에서 성과가 있었다. 2020년 코로나19의 영향으로 제약업종 공급망에는 차질이 있었지만 생산량으로는 큰 감소가 없었으며, 본격적 백신 생산으로 인한 여파가 있을 수 있다.
보고서는 바이러스 벡터를 이용한 백신생산의 증가로 인해 벡터 생산 분야에 긍정적 영향이 있을 것으로 예상했다.
최근 후지필름은 20억 달러를 세포배양공장에 투자했고 써모피셔는 8억 8000만 달러에 벡터 생산업체 혼젠(Honegen)을 인수했으며 싸이티바는 생산 캐파 확장에 5억 달러 투자를 계획 중이다.
다만, 세포·유전치료제의 경우 제조공정이 복잡하고 규제 정책이 많기 때문에 산업 성장이 원활하지 않을 수 있다는 의견이다. 대부분의 CMC 가이드라인은 세포·유전자 치료의 복잡성에 적합하지 않아 개선이 필요하기 때문이다.
재생의료연합에서는 2021년 AAV(adeno-associated virus) 벡터 제조사 설계기반품질(QbD) 적용 사례조사를 추진할 예정이다. 또 체외 세포 유전자편집 규제관리 등 유전자 편집과 관련된 의견을 WHO를 통해 국제적으로 전파할 예정이다.
전 세계적으로 1220건의 재생의료 임상이 이뤄지는 것으로 파악됐으며 152건은 3상 진행 중에 있다. 올해 들어 미국, 유럽 등에서 최소 8개의 재생의약품 허가가 기대해 볼 수도 있다는 예상이다.
미 FDA와 유럽 EMA에 따르면 2025년까지 각 기관별 연 10~20건의 세포·유전자 치료제를 승인할 것으로 예상하고 있다. 미국 FDA의 RMAT이나 유럽 EMA의 PRIME과 같은 첨단재생의료 치료제 패스트트랙 제도는 파이프라인 개발을 촉진하고 있다.
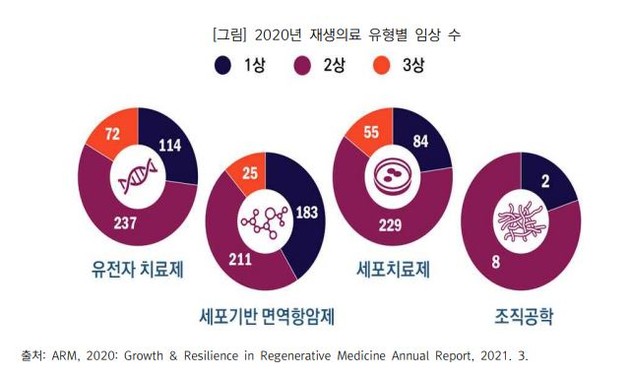
유전자치료제의 경우 임상 2상에 237건, 임상 3상에 72건이 진행되고 있다. 세포기반 면역함암제의 경우 임상 2상에 211건, 임상 3상에 25건이 진행되고 있는 등 많은 첨단바이오의약품이 임상 중후반 단계에 와 있다.

재생의료 산업 2024년까지 768억달러 성장
재생의료연합 보고서에 따르면 전 세계적으로 재생의료 산업은 코로나19 팬데믹으로 인한 경제 불황 속에서도 가파르게 성장하고 있는 것으로 확인된다. 특히 면역세포치료제 유전자치료제 영역의 투자 사례와 임상시험 비중이 높은 편이다.
이는 재생의료(첨단바이오의약품) 산업의 방향이 체세포, 줄기세포기반 산업에서 면역세포치료제, 유전자치료제 산업 중심으로 변화되고 있는 것으로 볼 수 있다.
다시 말해 재생의료산업의 범위가 손상된 인체세포와 조직, 장기를 대체하거나 재생시켜 정상적으로 기능하게 만드는 의료 산업의 범위에서 손상된 인체 부위의 재생과 세포의 기능을 촉진하는 산업으로 개념이 넓혀지고 있다는 뜻이다.
해외 시장조사 기관에서도 전 세계 재생의료(첨단바이오의약품) 산업은 2018년 250억 달러에서 2024년까지 768억달러 규모로 연평균 19.8% 성장할 것으로 전망하고 있다.
첨단바이오의약품 시장의 높은 성장 가능성과 선진국 규제기관의 패스트트랙제도로 인해 세포기반 면역항암제, 유전자치료제, 세포치료제에 대한 기업들의 연구개발과 생산 수요가 급증할 가능성이 있다. 이에 따라 제품 생산의 일시적 병목현상이 발생할 가능성이 있고 세포치료제·유전자치료제 위탁개발생산기업(CDMO)의 역할이 중요해질 것으로 보인다.
한편 국내 첨단바이오의약품 산업은 다수의 특허를 출원함으로서 그간 양적 성장을 해왔지만, 상대적으로 해외출원비율이 낮고 특허 영향력이 적어 글로벌 시장에서 경쟁력이 낮은 편으로 분석되고 있다. 이 때문에 국내 첨단바이오의약품 산업 경쟁력 확보와 글로벌 진출을 위해서는 질적으로 우수한 연구개발 성과를 선별해 글로벌 지식재산권을 확보하기 위한 전략이 요구된다.
바이오협회 관계자는 “국내에서도 이러한 글로벌 동향을 반영해 첨단바이오의약품의 임상개발과 심사의 신속한 절차를 진행할 수 있도록 패스트트랙 제도를 활성화해 국내 기업들의 연구개발을 촉진할 수 있도록 지원하고, 첨단바이오의약품의 국내외 연구개발 및 생산 수요에 대응하고 해외기업들과 경쟁할 수 있는 국내 CDMO의 역량 강화가 필요하다”는 의견을 밝혔다.
이원식 기자의 전체기사 보기
Copyright @보건신문 All rights reserved.