식의약당국이 규제과학 전문성을 바탕으로 국내 개발 바이오시밀러에 대한 체계적인 컨설팅을 제공해 신속하게 제품화될 수 있도록 지원하기로 했다.
식품의약품안전처는 국내 개발 바이오시밀러의 제품개발 성공률을 높이고 제품 출시를 앞당겨 수출을 지원하기 위해 '2023년 바이오시밀러 제품화 지원단'(이하 지원단)을 운영한다.
지원단은 비임상, 임상, 허가 등 전 주기에 걸쳐 국내 바이오시밀러 개발 업체가 겪는 어려움과 문제점에 대해 맞춤형으로 상담을 제공할 계획이다.
관심 있는 업체는 언제든 신청할 수 있으며, 유전자재조합의약품과 이메일 recombinant@korea.kr로 신청하면 된다. 내부 평가를 거쳐 최종 선정된 업체에 대해서는 신청 내용에 따라 품목별, 단계별 전담 상담팀을 구성해 맞춤형 밀착 상담을 제공한다.
지원단은 주요 바이오의약품의 특허 만료기한이 도래함에 따라 바이오시밀러 시장이 급격하게 성장할 것으로 예상하고 2020년부터 국내 바이오시밀러 개발 업체를 맞춤형으로 지원해오고 있다.
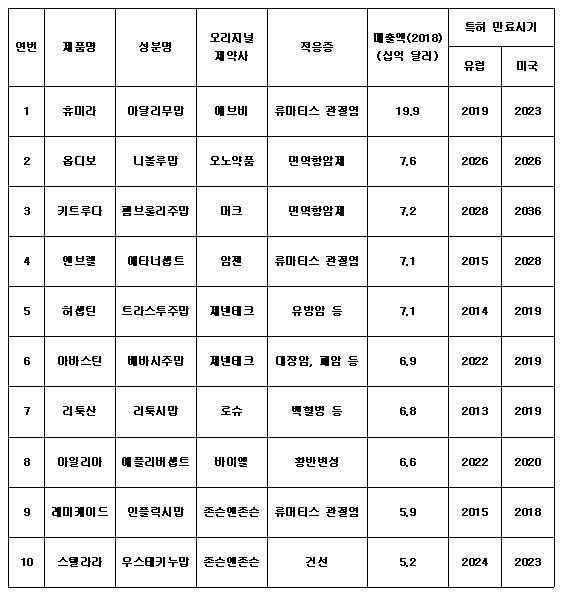
참고로 2019년부터 2023년까지 특허 만료 7개 품목(휴미라, 엔브렐, 허셉틴, 아바스틴, 리툭산(맙테라), 아일리아, 스텔라라)의 매출액은 2018년 기준 약 590억달러에 달한다.
식약처는 현재까지 총 5개 품목을 대상으로 맞춤형 상담을 진행했으며, 작년에는 루센티스(오리지널 의약품)에 대한 국산 바이오시밀러가 품목허가 되는 성과가 있었다. 종근당의 루센비에스주10밀리그램/밀리리터(라니비주맙)의 경우, 2020년 지원대상으로 선정된 후 개발 전략 상담을 총 3회 제공했고 지난 해 10월 제조판매 품목허가를 받았다.
식약처는 국산 신기술이 혁신제품이 돼 세계시장을 선도할 수 있도록 국내 규제를 글로벌 스탠다드화 하는 동시에, R&D 코디, 규제 전문가 밀착 상담, 글로벌 기준 우선 적용, 신속심사 등을 제공하는 브리지(BRIDGE) 프로젝트를 추진하고 있다.
특히 '바이오시밀러 제품화 지원단'과 같은 규제 전문가가 밀착 상담을 제공함으로써 제품개발 시 시행착오를 줄이는 데 도움을 줄 뿐만 아니라 허가·심사에 대한 예측성도 높이고 있다.
이원식 기자의 전체기사 보기
Copyright @보건신문 All rights reserved.